针对肿瘤研究的认知局限:引入深度神经网络重塑诊断精度
在生物医学研究领域,长期存在一个核心假设:如果深度神经网络能够理解人类语言的复杂上下文,那么其架构同样应当能够理解生物分子序列的逻辑。基于这一假设,科研团队将BERT模型应用于单细胞RNA测序数据的分析,试图解决传统方法在处理大规模、多维度生物数据时的局限性。这一实验性尝试,旨在通过算法的泛化能力,弥补传统人工注释在稳定性与可扩展性上的短板。
逻辑推理过程显示,单细胞测序数据具有高度的非结构化特征,传统的统计学方法往往难以处理其中的批次效应与技术噪声。引入Transformer架构后,模型通过在大规模公开数据集上的预训练,成功捕捉到了基因表达的全局规律。这种方法不再单纯依赖于已知的标志性基因,而是通过学习全基因组的表达模式,实现了对细胞类型的自动化精准识别。
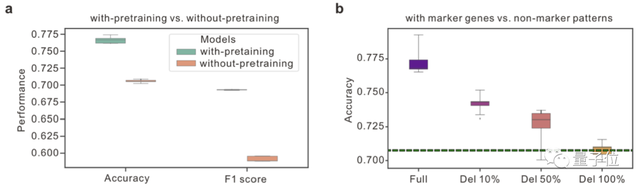
在实验设计阶段,研究人员选取了覆盖多种人体器官和主流测序技术的大规模数据集进行验证。结果分析表明,该模型在处理极具挑战性的外周血细胞亚型细分任务时,表现出了显著的性能提升。这一结论验证了深度神经网络在生物信息学领域的可行性,证明了通过算法优化可以有效提升细胞注释的准确度与稳定性,从而为后续的临床应用奠定了技术基础。
实现临床诊断的精准化应用
将该模型应用于临床场景,是其价值转化的关键一步。通过对患者肿瘤微环境的精细化分析,医生能够更清晰地识别出肿瘤细胞的异质性,从而筛选出更具针对性的治疗靶点。这种基于客观数据的分析流程,减少了人为因素对诊断结果的干扰,提升了辅助诊断的可靠性,为实现个性化医疗提供了强有力的技术支撑。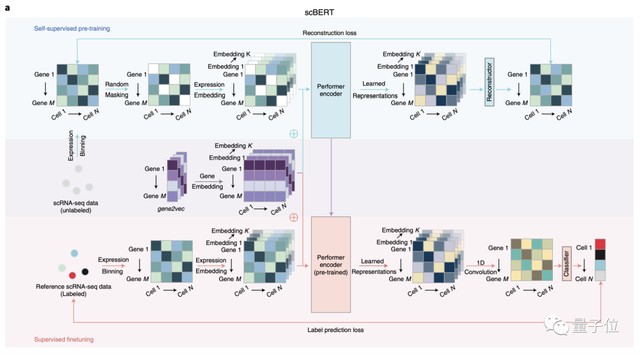
在未来的临床工作流中,该工具的价值将进一步凸显。随着算法在更多病种中的验证与优化,其不仅能够辅助医生进行疾病的早期筛查,还能在药物研发过程中帮助科研人员快速筛选潜在的耐药性机制。这种从技术到临床的平滑过渡,展示了人工智能在提升医疗质量、降低诊疗成本方面的巨大潜力,为现代医学的发展提供了新的路径。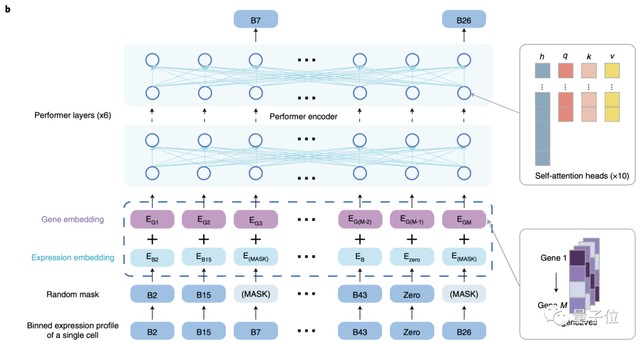
提升生物数据处理的规范性
标准化是推动生物医学技术走向成熟的必经之路。通过开源模型与数据集,研究团队不仅提供了一种高效的分析工具,更推动了单细胞测序领域数据处理规范的建立。这种透明化的技术共享,降低了科研门槛,使得全球的研究人员能够在统一的技术框架下开展合作,共同推动生命科学领域的知识积累与技术进步,确保了科研成果的高效转化与应用推广。